Senyawa Organologam
Senyawa organologam adalah senyawa di mana atom-atom karbon dari gugus organik terikat kepada atom logam. Contoh, suatu aloksida seperti (C3H7O)4Ti tidaklah dianggap sebagai suatu senyawa organologam karena gugus organiknya terikat pada Ti melalui oksigen, sedangkan C6H5Ti(OC3H7)3 karena terdapat satu ikatan langsung antara karbon C dari gugus fenil dengan logam Ti.HH Istilah organologam biasanya didefenisikan agak longgar, dan senyawaan dari unsur-unsur seperti Boron, fosfor, dan silikon semuanya mirip logam. Tetapi untuk senyawa yang mengandung ikatan antara atom logam dengan oksigen, belerang, nitrogen, ataupun dengan suatu halogen tidak termasuk sebagai senyawa organologam. Dari bentuk ikatan pada senyawa organologam, senyawa ini dapat dikatakan sebagai jembatan antara kimia organik dan anorganik. Pada dasarnya Organologam prinsipnya yaitu atom-atom Karbon dari gugus organik terikat kepada atom logam. Konsep ini yang mendasari Organologam, sehingga banyak cara untuk menghasilkan ikatan-ikatan logam pada Carbon yang berguna bagi kedua logam transisi dan non-transisi.Beberapa yang lebih penting adalah sebagai berikut:1. Reaksi Logam langsung ; sintesis yang paling awal oleh ahli kimia Inggris, Frankland dalam tahun 1845 adalah interaksi antara Zn dan suatu alkil Halida. Adapun yang lebih berguna adalah penemuan ahli kimia Perancis, Grignard yang dikenal sebagai pereaksi Grignard. Contohnya interaksi Magnesium dan alkil atau aril Halida dalam eter:Mg + CH3I → CH3MgIInteraksi langsung alkil atau aril Halida juga terjadi dengan Li, Na, K, Ca, Zn dan Cd.2. Penggunaan zat pengalkilasi. Senyawa ini dimanfaatkan untuk membuat senyawa organologam lainnya. Kebanyakan Halida nonlogam dan logam atau turunan Halida dapat dialkilasi dalam eter atau pelarut hidrokarbon, misalnya :PCl3 + 3C6H5MgCl → P(C6H5)3 + 3MgCl2VOCl3 + 3(CH3)3SiCH2MgCl → VO(CH2SiMe3)3 + 3MgCl23. Interaksi Hidrida Logam atau nonlogam dengan alkena atau alkuna.4. Reaksi Oksidatif adisi. Reaksi yang dikenal sebagai reaksi Oksa dimana Alkil atau Aril Halida ditambahkan pada senyawa logam transisi Koordinasi tidak jenuh menghasilkan ikatan logam Karbon. Contohnya:RhCl(PPh3)3 + CH3I → RhClI(CH3)(PPh3)2 + PPh35. Reaksi Insersi yaitu reaksi yang menghasilkan ikatan-ikatan dengan Karbon, sebagai contoh:SbCl5 + 2HC CH→Cl3Sb(CH=CHCl)2Grignard reagentReaksi Grignard adalah reaksi kimia organologam di mana alkil - atau Aril-magnesium halides (reagen Grignard) menambah gugus karbonil Aldehida atau keton. Reaksi ini adalah alat penting untuk pembentukan ikatan antar karbon. Reaksi Halida organik dengan magnesium bukan reaksi Grignard, tetapi menyediakan peraksi Grignard. Pereaksi Grignard memiliki rumus umum RMgX dimana X adalah sebuah halogen, dan R adalah sebuah gugus alkil atau aril (berdasarkan pada sebuah cincin benzen). Pereaksi Grignard sederhana bisa berupa CH3CH2MgBr.
Sebuah contoh dari reaksi grignard
Mekanisme dari reaksi Grignard:
ADISI ORGANOMETALIK
Reaksi Pembuatan Senyawa OrganologamTerdapat banyak cara untuk membentuk ikatan-ikatan logam antara karbon dengan logam transisi dan nontransisi. Beberapa yang penting adalah sebagai berikut :1. Reaksi logam langsungMg + CH3I → CH3MgI2. Penggunaan zat pengalkilasiPCl3 + 3C6H5MgCl → P(C6H5)3 + 3MgCl2VOCl3 + 3(CH3)SiCH2MgCl → VO(CH2SiMe3)3 + 3MgCl2PtCl2(Pet3)2 + CH3MgCl → PtCl(CH3)(Pet2)2 + MgCl23. Interaksi hidrida logam atau nonlogam dengan alkena atau alkuna1/2 B2H6 + 3 C=C → B-(C=C)34. Reaksi oksidasi AdidiDimana alkil atau aril halida ditambahkan kepada senyawa logam transisi terkoordinasi tidak jenuh menghasilkan ikatan logam karbon.RhCl(PPh3)3 + CH3I → RhClI(CH3)(PPh3)2 + PPh35. Reaksi Inseri
Reaksi-Reaksi Senyawa Organologam
- Substitusi: Reaksi penggantian suatu gugus dengan gugus lain2. Eliminasi
- Reaksi penggantian ikatan, dari ikatan tunggal menjadi rangkap.

- Oksidasi
4. Adisi
Reaksi adisi adalah reaksi pengubahan senyawa yang berikatan rangkap (tak jenuh) menjadi senyawa yang berikatan tunggal (jenuh) dengan cara menambahkan atom dari senyawa lain. Reaksi adisi hanya dapat terjadi pada senyawa yang memiliki ikatan rangkap. Atau dengan kata lain reaksi adisi adalah reaksi penambahan suatu atom atau gugus atom kedalam senyawa.
Reaksi Grignard
Reaksi Grignard adalah reaksi kimia organologam di mana alkil - atau Aril-magnesium halides (reagen Grignard) menambah gugus karbonil Aldehida atau keton. Reaksi ini adalah alat penting untuk pembentukan ikatan antar karbon. Reaksi Halida organik dengan magnesium bukan reaksi Grignard, tetapi menyediakan peraksi Grignard. Pereaksi Grignard memiliki rumus umum RMgX dimana X adalah sebuah halogen, dan R adalah sebuah gugus alkil atau aril (berdasarkan pada sebuah cincin benzen). Pereaksi Grignard sederhana bisa berupa CH3CH2MgBr.
Mekanisme Reaksi :
Reagen Grignard berfungsi sebagai nukleofil, menyerang atom karbon elektrofilik yang hadir dalam ikatan polar gugus karbonil. Penambahan pereaksi Grignard untuk karbonil biasanya hasil melalui keadaan transisi enam-beranggota cincin.
Namun, dengan pereaksi Grignard terhalang, reaksi dapat melanjutkan dengan transfer elektrontunggal. Jalur serupa diasumsikan untuk reaksi lain dari reagen Grignard, misalnya, dalam pembentukan ikatan antara karbon-fosfor, timah-karbon, karbon-silikon, boron-karbon dan karbon-heteroatom.
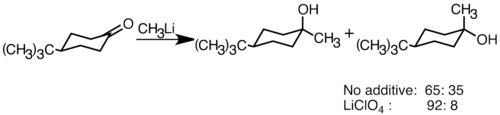
Reagen organolitik nukleofilik dapat menambah ikatan ganda karbida elektrofilik untuk membentuk ikatan karbon-karbon. Mereka dapat bereaksi dengan aldehida dan ketonuntuk menghasilkan alkohol . Penambahan berlangsung terutama melalui penambahan polar, di mana spesies organolitik nukleofilik menyerang dari arah khatulistiwa, dan menghasilkan alkohol aksial. Penambahan garam lithium seperti LiClO 4 dapat meningkatkan stereoselektivitas reaksi.
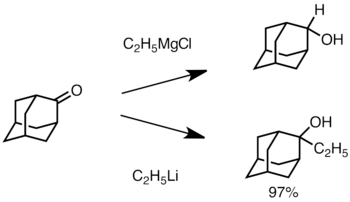
Ketika keton terhambat secara sterik, menggunakan pereaksi Grignard sering menyebabkan reduksi gugus karbonil, bukan penambahan. Namun, reagen alkyllithium cenderung mengurangi keton, dan dapat digunakan untuk mensintesis alkohol tersubstitusi. Di bawah ini adalah contoh dari penambahan ethyllithium ke adamantone untuk menghasilkan alkohol tersier.
Organolithium reagen juga lebih unggul daripada reagen Grignard dalam kemampuannya untuk bereaksi dengan asam karboksilat untuk membentuk keton. Reaksi ini dapat dioptimalkan dengan hati-hati mengontrol jumlah penambahan reagen organolitium, atau menggunakan trimethylsilyl chloride untuk memuaskan pereaksi lithium berlebih. Cara yang lebih umum untuk mensintesis keton adalah melalui penambahan reagen organolitium ke Weinreb amides (N-methoxy-N-methyl amides). Reaksi ini menghasilkan keton ketika pereaksi organolithium digunakan secara berlebihan, karena chelation ion litium antara oksigen N-metoksi dan oksigen karbonil, yang membentuk intermediet tetrahedral yang runtuh pada kerja asam.
Organolithium reagen juga dapat bereaksi dengan karbon dioksida untuk membentuk asam karboksilat .
Dalam kasus substrat enone , di mana dua situs penambahan nukleofilik dimungkinkan (1,2 selain karbon karbonil atau 1,4 konjugat selain karbon β), spesies organolitium yang paling reaktif mendukung tambahan 1,2, namun, ada beberapa cara untuk mendorong reagen organolithium untuk menjalani penambahan konjugasi. Pertama, karena adduct 1,4 kemungkinan adalah spesies yang lebih termodinamik, penambahan konjugasi dapat dicapai melalui equilibrium (isomerisasi dari dua produk), terutama ketika nukleofil lithium lemah dan penambahan 1,2 reversibel. Kedua, menambahkan ligan donor ke dalam reaksi membentuk spesies lithium heteroatom-stabil yang mendukung penambahan 1,4 konjugasi. Dalam satu contoh, penambahan tingkat rendah HMPA ke pelarut mendukung penambahan 1,4. Dengan tidak adanya ligan donor, lithium kation terkoordinasi erat dengan atom oksigen, namun, ketika kation lithium dilarutkan oleh HMPA, koordinasi antara karbonil oksigen dan ion lithium melemah. Metode ini umumnya tidak dapat digunakan untuk mempengaruhi regioselektivitas reagen alkil dan arilithium.
Organolithium reagen juga dapat melakukan penambahan nukleofilik enantioselektif untuk karbonil dan turunannya, sering dengan adanya ligan kiral. Reaktivitas ini secara luas diterapkan dalam sintesis industri senyawa farmasi. Contohnya adalah sintesis Merck dan Dupont Efavirenz , suatu penghambat transcriptase reverse HIV yang poten.Lithium acetylide ditambahkan ke keton prokiral untuk menghasilkan produk alkohol kiral. Struktur intermediet reaksi aktif ditentukan oleh studi spektroskopi NMR dalam keadaan larutan dan kristalografi sinar-X dari keadaan padat menjadi kubik 2: 2 tetramer.
- Bagaimana aplikasi senyawa organologam sehingga berperan vital dalam kehidupan?
- Bagaimana cara kerja organometalik sehingga dapat dipakai sebagai anti knocking dalam gasoline?
- Bagaimana cara membuat reaksi pembentukan organolitium sehingga dapat bereaksi dengan suatu karbokation, dan rantai atom karbon bertambah panjang 4x ?! (dengan alkil halida, dengan suatu ester, dengan suatu erpoksida dan dengan suatu keton)






Baiklah saya akan menjawab no 1
BalasHapusSenyawa organologam banyak digunakan sebagai Katalis, Aplikasi Senyawa organologam dalam katalisis memang menjadi faktor meningkatnya minat peneliti terhadap organologam. Melihat sejarah industrinya, katalis organologam memiliki sejarah panjang dalam produksi senyawa organik dan polimer.
Aplikasi penyulingan Nikel pada awal 1880-an contohnya, Ludwig moond mampu menunjukkan bagaimana Ni mentah dapat dimurnikan dengan CO untuk menguapkan Ni dalam bentuk Ni (CO)4 sebagai uap kemudian dapat dipanaskan untuk memperoleh Ni murni [1].
Senyawa organologam juga mengambil peran dalam bidang kesehatan, banyak sekali aplikasi pemanfaatan senyawa organologam di bidang kesehatan salah satunya adalah Haemoglobin. Haemoglobin (Hb) merupakan senyawa metalloprotein yang berperan mengantarkan Oksigen ke seluruh tubuh, Haemoglobin juga berperan dalam proses transportasi gas lain seperti karbondioksida [3].
Baiklah saya akan mencoba menjawab permasalahan yang pertama yaitu Kimia arnologam adalah ilmu yang mempelajari senyawa yang mengandung ikatan antara karbon dan logam. Dalam kimia anarlogam terdapat perpaduan antara kimia anorganik dan organik, senyawa anarlogam antara lain sebagai katalis dalam pengolahan hasil minyak bumi dan dalam prosess produksi polimer organik. Senyawa organologam secara luas digunakan baik secara stoikiometrik dalam penelitian dan reaksi kimia industri, maupun dalam peran katalis untuk meningkatkan laju reaksi tersebut (misalnya, seperti dalam katasilsitis), di mana molekul target termasuk polimer, obat-obatan, dan banyak jenis produk praktis lainnya.
BalasHapusKimia organologam adalah studi mengenaisenyawa organologam, senyawa kimia yang mengandung setidaknya satu ikatan kimiaantara atom karbon dari sebuah molekul organik dan logam, termasuk alkali, alkali tanah, dan logam transisi, dan terkadang diperluas untuk mencakup metaloid seperti boron, silikon, dan timah, pula.[1] Selain ikatan untuk fragmen atau molekul organil, ikatan dengan karbon 'anorganik', seperti karbon monoksida (karbonil logam), sianida, atau karbida, umumnya dianggap organologam juga. Beberapa senyawa yang terkait sepertilogam transisi hidrida dan kompleks logam fosfina sering dimasukkan dalam diskusi senyawa organologam, meskipun secara tegas, mereka tidak selalu merupakan organologam.
Saya skan menjawab pertanyaan no 1 Dalam kimia anarlogam terdapat perpaduan antara kimia anorganik dan organik, senyawa anarlogam antara lain sebagai katalis dalam pengolahan hasil minyak bumi dan dalam prosess produksi polimer organik. Senyawa organologam secara luas digunakan baik secara stoikiometrik dalam penelitian dan reaksi kimia industri, maupun dalam peran katalis untuk meningkatkan laju reaksi tersebut (misalnya, seperti dalam katasilsitis), di mana molekul target termasuk polimer, obat-obatan, dan banyak jenis produk praktis lainnya.
BalasHapusSaya skan menjawab pertanyaan no 1 Dalam kimia anarlogam terdapat perpaduan antara kimia anorganik dan organik, senyawa anarlogam antara lain sebagai katalis dalam pengolahan hasil minyak bumi dan dalam prosess produksi polimer organik. Senyawa organologam secara luas digunakan baik secara stoikiometrik dalam penelitian dan reaksi kimia industri, maupun dalam peran katalis untuk meningkatkan laju reaksi tersebut (misalnya, seperti dalam katasilsitis), di mana molekul target termasuk polimer, obat-obatan, dan banyak jenis produk praktis lainnya.
BalasHapusSaya skan menjawab pertanyaan no 1 Dalam kimia anarlogam terdapat perpaduan antara kimia anorganik dan organik, senyawa anarlogam antara lain sebagai katalis dalam pengolahan hasil minyak bumi dan dalam prosess produksi polimer organik. Senyawa organologam secara luas digunakan baik secara stoikiometrik dalam penelitian dan reaksi kimia industri, maupun dalam peran katalis untuk meningkatkan laju reaksi tersebut (misalnya, seperti dalam katasilsitis), di mana molekul target termasuk polimer, obat-obatan, dan banyak jenis produk praktis lainnya.
BalasHapusSaya skan menjawab pertanyaan no 1 Dalam kimia anarlogam terdapat perpaduan antara kimia anorganik dan organik, senyawa anarlogam antara lain sebagai katalis dalam pengolahan hasil minyak bumi dan dalam prosess produksi polimer organik. Senyawa organologam secara luas digunakan baik secara stoikiometrik dalam penelitian dan reaksi kimia industri, maupun dalam peran katalis untuk meningkatkan laju reaksi tersebut (misalnya, seperti dalam katasilsitis), di mana molekul target termasuk polimer, obat-obatan, dan banyak jenis produk praktis lainnya.
BalasHapusDalam kimia anarlogam terdapat perpaduan antara kimia anorganik dan organik, senyawa anarlogam antara lain sebagai katalis dalam pengolahan hasil minyak bumi dan dalam prosess produksi polimer organik. Senyawa organologam secara luas digunakan baik secara stoikiometrik dalam penelitian dan reaksi kimia industri, maupun dalam peran katalis untuk meningkatkan laju reaksi tersebut (misalnya, seperti dalam katasilsitis), di mana molekul target termasuk polimer, obat-obatan, dan banyak jenis produk praktis lainnya.
BalasHapusKimia organologam adalah studi mengenaisenyawa organologam, senyawa kimia yang mengandung setidaknya satu ikatan kimiaantara atom karbon dari sebuah molekul organik dan logam, termasuk alkali, alkali tanah, dan logam transisi, dan terkadang diperluas untuk mencakup metaloid seperti boron, silikon, dan timah, pula.[1] Selain ikatan untuk fragmen atau molekul organil, ikatan dengan karbon 'anorganik', seperti karbon monoksida (karbonil logam), sianida, atau karbida, umumnya dianggap organologam juga.
Baiklah saya akan mencoba menjawab permasalahan yang pertama yaitu Kimia arnologam adalah ilmu yang mempelajari senyawa yang mengandung ikatan antara karbon dan logam. Dalam kimia anarlogam terdapat perpaduan antara kimia anorganik dan organik, senyawa anarlogam antara lain sebagai katalis dalam pengolahan hasil minyak bumi dan dalam prosess produksi polimer organik. Senyawa organologam secara luas digunakan baik secara stoikiometrik dalam penelitian dan reaksi kimia industri, maupun dalam peran katalis untuk meningkatkan laju reaksi tersebut (misalnya, seperti dalam katasilsitis), di mana molekul target termasuk polimer, obat-obatan, dan banyak jenis produk praktis lainnya.
BalasHapusSaya skan menjawab pertanyaan no 1 Dalam kimia anarlogam terdapat perpaduan antara kimia anorganik dan organik, senyawa anarlogam antara lain sebagai katalis dalam pengolahan hasil minyak bumi dan dalam prosess produksi polimer organik. Senyawa organologam secara luas digunakan baik secara stoikiometrik dalam penelitian dan reaksi kimia industri, maupun dalam peran katalis untuk meningkatkan laju reaksi tersebut (misalnya, seperti dalam katasilsitis), di mana molekul target termasuk polimer, obat-obatan, dan banyak jenis produk praktis lainnya.
BalasHapussaya akan menjawab permasalahan yg ke 2
BalasHapusIkatan karbon dengan logam dalam senyawa organometalik umumnya bersifat sebagian ionic dan sebagian kovalen. Jika ikatan logam-C bersifat ion maka hal ini disebabkan karena logam yang dipakai sangat bersifat elektropositif seperti logam alkali, atau ada dalam bentuk karbanion. Sedangakn sifat ionic ikatan logam-C dalam logam transisi dan metalloid sangat rendah tergantung dari elektronegatifitas logam itu sendiri. Sifat ionic dan kovalen ikatan logam-C amat penting disebabkan ini memerankan peranan dalam kestabilan didalam larutan.
Organometalik memiliki peranan yang penting dalam sintesis kimia dan katalis. Sepeerti tetra etil lead (TEL) dipakai sebagai anti knocking dalam gasoline akan tetapi sekarang banyak diganti oleh ferosena atau methylcyclopentadienyl manganese tricarbonyl. Organometalik dari litium atau seng bersifat basa dan bersifat sebagai reduktor dan banyak dipakai dalam sintesis kimia organic. ButilLitium (gambar) adalah contoh organometalik yang banyak dipakai dalam sintesis.
Nomor 1
BalasHapusSenyawa organologam banyak digunakan sebagai Katalis, Aplikasi Senyawa organologam dalam katalisis memang menjadi faktor meningkatnya minat peneliti terhadap organologam. Melihat sejarah industrinya, katalis organologam memiliki sejarah panjang dalam produksi senyawa organik dan polimer.
Aplikasi penyulingan Nikel pada awal 1880-an contohnya, Ludwig moond mampu menunjukkan bagaimana Ni mentah dapat dimurnikan dengan CO untuk menguapkan Ni dalam bentuk Ni (CO)4 sebagai uap kemudian dapat dipanaskan untuk memperoleh Ni murni.
Saya skan menjawab pertanyaan no 1 Dalam kimia anarlogam terdapat perpaduan antara kimia anorganik dan organik, senyawa anarlogam antara lain sebagai katalis dalam pengolahan hasil minyak bumi dan dalam prosess produksi polimer organik. Senyawa organologam secara luas digunakan baik secara stoikiometrik dalam penelitian dan reaksi kimia industri, maupun dalam peran katalis untuk meningkatkan laju reaksi tersebut (misalnya, seperti dalam katasilsitis), di mana molekul target termasuk polimer, obat-obatan, dan banyak jenis produk praktis lainnya.
BalasHapus