Amine
| Primer (1 °) amina | Amina sekunder (2 °) | Tersier (3 °) amina |
|---|---|---|
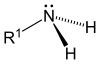 |  |  |
- Amina primer (1 °) - Amina primer muncul ketika salah satu dari tiga atom hidrogen dalam amonia diganti oleh gugus alkil atau aromatik . Amilium alkil utama yang penting meliputi, metilamin , sebagian besar asam amino , dan tris penyangga , sedangkan amina aromatik primer termasuk anilin .
- Amina sekunder (2 °) - Amina sekunder memiliki dua substituen organik (alkil, aril atau keduanya) terikat ke nitrogen bersama dengan satu hidrogen. Perwakilan penting termasuk dimethylamine , sementara contoh amina aromatik akan diphenylamine .
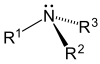
- Tersier (3 °) amina -Dalam amina tersier, nitrogen memiliki tiga substituen organik. Contohnya termasuk trimethylamine , yang memiliki bau khas mencurigakan, dan EDTA .
- Amina siklik - Amina siklik adalah amina sekunder atau tersier. Contoh-contoh amina siklik termasuk cincin-3 aziridine dan cincin piperidin beranggota enam. N -methylpiperidine dan N -phenylpiperidine adalah contoh amina tersier siklik.
| Amina lebih rendah diberi nama dengan akhiran -amine . | Amina yang lebih tinggi memiliki amino awalan sebagai kelompok fungsional. IUPAC namun tidak merekomendasikan konvensi ini, Tetapi lebih suka bentuk alkanamine, misalnya pentan-2-amina. |
3 )> amonium sekunder ( R)
2 NH +
2 )> amonium tersier (R 3 NH + ). Amina alifatik kecil menunjukkan kelarutan yang signifikan dalam banyak pelarut , sedangkan yang memiliki substituen besar adalah lipofilik. Amina aromatik, seperti anilin , memiliki elektron pasangan elektron bebas yang terkonjugasi ke cincin benzen, sehingga kecenderungan mereka untuk terlibat dalam ikatan hidrogen berkurang. Titik didihnya tinggi dan kelarutannya dalam air rendah.
Identifikasi spektroskopi
Struktur
Alkyl amines
 | ⇌ |  |
| Pembalikan amina. Sepasang titik melambangkan pasangan elektron tunggal pada atom nitrogen. | ||
Dasar-dasar
| Alkylamine atau aniline | pK a amina terprotonasi | K b |
|---|---|---|
| methylamine (MeNH 2 ) | 10.62 | 4.17E-04 |
| dimethylamine (Me 2 NH) | 10.64 | 4.37E-04 |
| trimethylamine (Me 3 N) | 9,76 | 5.75E-05 |
| ethylamine (EtNH 2 ) | 10.63 | 4.27E-04 |
| aniline (PhNH 2 ) | 4,62 | 4.17E-10 |
| 4-methoxyaniline (4-MeOC 6 H 4 NH 2 ) | 5,36 | 2.29E-09 |
| N, N-Dimethylaniline (PhNMe 2 ) | 5,07 | 1.17E-09 |
| 3-Nitroaniline (3-NO 2 -C 6 H 4 NH 2 ) | 2.46 | 2.88E-12 |
| 4-Nitroaniline (4-NO 2 -C 6 H 4 NH 2 ) | 1 | 1.00E-13 |
| 4-trifluoromethylaniline (CF 3 C 6 H 4 NH 2 ) | 2,75 | 5.62E-12 |
- Sifat elektronik dari substituen (gugus alkil meningkatkan kebasaan, gugus aril menguranginya).
- Tingkat solvasi amon terprotonasi, yang meliputi halangan sterik oleh kelompok-kelompok pada nitrogen.
Efek solvasi
Sintesis
Alkilasi
ROH + NH 3 → RNH 2 + H 2 O
RX + 2 R′NH 2 → RR′NH + [RR′NH 2 ] X
Rute reduktif
Metode khusus
Reaksi
Alkilasi, asilasi, dan sulfonasi
Substituen -NH 2 disebut gugus amino.
Senyawa dengan atom nitrogen yang melekat pada gugus karbonil , sehingga memiliki struktur R-CO-NR′R ″, disebut amida dan memiliki sifat kimia yang berbeda dari amina.
Klasifikasi amina
Amina dapat diklasifikasikan menurut sifat dan jumlah substituen pada nitrogen. Amina alifatik hanya mengandung substituen H dan alkil. Amina aromatik memiliki atom nitrogen yang terhubung ke cincin aromatik .
Amina, alkil dan aril, disusun menjadi tiga subkategori (lihat tabel) berdasarkan jumlah atom karbon yang berdekatan dengan nitrogen:
Subkategori keempat ditentukan oleh konektivitas dari substituen yang melekat pada nitrogen:
Juga dimungkinkan untuk memiliki empat substituen organik pada nitrogen. Spesies ini bukan amina tetapi kation amonium kuaterner dan memiliki pusat nitrogen bermuatan.Garam amonium kuarter ada dengan banyak jenis anion.
Amina diberi nama dengan beberapa cara. Biasanya, senyawa diberi awalan "amino-" atau akhiran: "-amine". Awalan " N -" menunjukkan substitusi pada atom nitrogen.Senyawa organik dengan banyak gugus amino disebut diamina, triamin, tetraamin, dan sebagainya.
Nama sistematis untuk beberapa amina umum:
Ikatan hidrogen secara signifikan mempengaruhi sifat amina primer dan sekunder. Misalnya, metil dan etil amina adalah gas dalam kondisi standar, sedangkan metil dan etilalkohol yang sesuai adalah cairan. Amina memiliki bau amonia yang khas, amina cair memiliki bau khas "amis".
Atom nitrogen memiliki pasangan elektron tunggal yang dapat mengikat H + untuk membentuk ion amonium R 3 NH + . Pasangan elektron tunggal diwakili dalam artikel ini oleh dua titik di atas atau di samping N. Kelarutan air amina sederhana ditingkatkan dengan ikatan hidrogen yang melibatkan pasangan elektron tunggal ini. Biasanya garam senyawa amonium menunjukkan urutan berikut kelarutan dalam air: amonium primer ( RNH +
Biasanya kehadiran gugus fungsi amina dideduksi oleh kombinasi teknik, termasuk spektrometri massa serta spektroskopi NMR dan IR. Sinyal 1H NMR untuk amina menghilang setelah perlakuan sampel dengan D2O. Dalam spektrum inframerah, amina primer menunjukkan dua band NH, sedangkan amina sekunder hanya menunjukkan satu.
Alkil amina secara karakteristik memiliki pusat nitrogen tetrahedral. Sudut CNC dan CNH mendekati sudut ideal 109 °. Jarak CN sedikit lebih pendek dari jarak CC.Penghalang energi untuk nitrogen inversi dari stereocenter adalah sekitar 7 kkal / mol untuk trialkilamin. Interkonversi telah dibandingkan dengan inversi payung terbuka menjadi angin kencang.
Amina dari tipe NHRR ′ dan NRR′R ″ adalah kiral : pusat nitrogen mengandung empat substituen yang menghitung pasangan elektron bebas. Karena penghalang rendah untuk inversi, amina dari tipe NHRR ′ tidak dapat diperoleh dalam kemurnian optik. Untuk amina tersier kiral, NRR′R ″ hanya dapat diselesaikan ketika R, R ′, dan R ″ kelompok dibatasi dalam struktur siklik seperti aziridine N-tersubtitusi ( garam amonium kuartener dapat dipecahkan).
Dalam amina aromatik ("anilin"), nitrogen sering mendekati planar karena konjugasi pasangan elektron bebas dengan substituen aril. Jarak CN juga lebih pendek. Dalam aniline, jarak CN sama dengan jarak CC.
Seperti amonia, amina adalah basa . Dibandingkan dengan hidroksida logam alkali, amina lebih lemah (lihat tabel untuk contoh asam konjugasi K a ).
Kebasaan amina bergantung pada:
Karena efek induktif, kebasaan amina mungkin akan meningkat dengan jumlah gugus alkil pada amina. Korelasi rumit karena efek solvasi yang berlawanan dengan tren untuk efek induktif. Efek solvasi juga mendominasi kebasaan amina aromatik (anilin). Untuk anilin, pasangan elektron bebas pada nitrogen mendelokalisasi ke dalam cincin, sehingga menurunkan kebasaan. Substituen pada cincin aromatik, dan posisi mereka relatif terhadap gugus amina, juga mempengaruhi kebasaan seperti yang terlihat dalam tabel.
Solvasi secara signifikan mempengaruhi kebasaan amina. Kelompok NH sangat berinteraksi dengan air, terutama dalam ion amonium. Akibatnya, kebasaan amonia ditingkatkan oleh 10 11 dengan solvasi. Kebenaran intrinsik amina, yaitu situasi di mana solvasi tidak penting, telah dievaluasi dalam fase gas. Dalam fase gas, amina menunjukkan dasar-dasar yang diprediksi dari efek pelepas elektron dari substituen organik. Jadi amina tersier lebih mendasar daripada amina sekunder, yang lebih mendasar daripada amina primer, dan akhirnya amonia paling tidak dasar. Urutan pK b (dasar dalam air) tidak mengikuti urutan ini. Demikian pula anilin lebih mendasar daripada amonia dalam fase gas, tetapi sepuluh ribu kali lebih sedikit dalam larutan encer.
Dalam pelarut polar aprotik seperti DMSO , DMF , dan asetonitril , energi solvasi tidak setinggi seperti pelarut polar protik seperti air dan metanol. Untuk alasan ini, dasar-dasar amina dalam pelarut aprotik ini hampir sepenuhnya diatur oleh efek elektronik.
Amina yang paling penting secara industri dibuat dari amonia oleh alkilasi dengan alkohol:
Berbeda dengan reaksi amina dengan alkil halida, metode industri adalah hijau sejauh bahwa coproduct adalah air. Reaksi amina dan amonia dengan alkil halida digunakan untuk sintesis di laboratorium:
Reaksi semacam itu, yang paling berguna untuk alkil iodida dan bromida, jarang digunakan karena tingkat alkilasi sulit dikendalikan. Selektivitas dapat ditingkatkan melalui reaksi Delépine , meskipun ini jarang digunakan pada skala industri.
Melalui proses hidrogenasi , nitril direduksi menjadi amina menggunakan hidrogen dengan adanya katalis nikel. Reaksi sensitif terhadap kondisi asam atau basa, yang dapat menyebabkan hidrolisis grup -CN. LiAlH 4 lebih umum digunakan untuk reduksi nitril pada skala laboratorium. Demikian pula, LiAlH 4 mengurangi amida untuk amina. Banyak amina dihasilkan dari aldehida dan keton melalui aminasi reduktif , yang dapat dilanjutkan secara katalitis atau stoikiometri.
Aniline (C 6 H 5 NH 2 ) dan turunannya disiapkan dengan reduksi nitroaromatics. Dalam industri, hidrogen adalah reduktan yang disukai, sedangkan di laboratorium, timah dan besi sering digunakan.
Banyak metode laboratorium yang ada untuk persiapan amina, banyak dari metode ini yang agak terspesialisasi.
Selain dari dasar mereka, reaktivitas dominan amina adalah nukleofilisitas mereka. Kebanyakan amina primer adalah ligan yang baik untuk ion logam untuk menghasilkan kompleks koordinasi . Amina dialkilasi oleh alkil halida. Asil klorida dan anhidrida asam bereaksi dengan amina primer dan sekunder untuk membentuk amida ( reaksi " Schotten-Baumann ").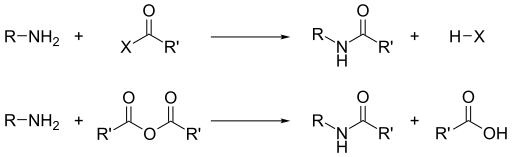

Demikian pula, dengan sulfonil klorida, seseorang memperoleh sulfonamid . Transformasi ini, yang dikenal sebagai reaksi Hinsberg , adalah tes kimia untuk kehadiran amina.
Karena amina bersifat mendasar, mereka menetralisir asam untuk membentuk garam amonium R 3 NH + yang sesuai. Ketika terbentuk dari asam karboksilat dan amina primer dan sekunder, garam-garam ini mengalami dehidrasi termal untuk membentuk amida yang sesuai.
![{\displaystyle {\underbrace {\ce {H-\!\!{\overset {\displaystyle R1 \atop |}{\underset {| \atop \displaystyle R2}{N}}}\!\!\!\!:}} _{amine}+\underbrace {\ce {R3-{\overset {\displaystyle O \atop \|}{C}}-OH}} _{\text{carboxylic acid}}->}\ \underbrace {\ce {{H-{\overset {\displaystyle R1 \atop |}{\underset {| \atop \displaystyle R2}{N+}}}-H}+R3-COO^{-}}} _{{\text{substituted-ammonium}} \atop {\text{carboxylate salt}}}{\ce {->[heat][dehydration]}}{\underbrace {\ce {{\overset {\displaystyle R1 \atop |}{\underset {| \atop \displaystyle R2}{N}}}\!\!-{\overset {\displaystyle O \atop \|}{C}}-R3}} _{amide}+\underbrace {\ce {H2O}} _{water}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ed9e4ee62efb585271572cbf0fd9149c90a400fd)
Diazotisasi
Konversi menjadi imina
RNH 2 + R ′ 2 C = O → R ′ 2 C = NR + H 2 O
R ′ 2 C = NR + H 2 → R ′ 2 CH-NHR
R 2 NH + R ′ (R ″ CH 2 ) C = O → R ″ CH = C (NR 2 ) R ′ + H 2 O
Ikhtisar
Aktivitas biologis
3 ) adalah moieties bermuatan positif yang paling umum dalam protein , khususnya pada asam amino lisin . DNA polimer anionik biasanya terikat pada berbagai protein kaya amina. Selain itu, terminal bermuatan amonium primer pada lisin membentuk jembatan garam dengan gugus karboksilat dari asam amino lainnya dalam polipeptida , yang merupakan salah satu pengaruh utama pada struktur tiga dimensi protein.
Konversi menjadi imina
RNH 2 + R ′ 2 C = O → R ′ 2 C = NR + H 2 O
R ′ 2 C = NR + H 2 → R ′ 2 CH-NHR
R 2 NH + R ′ (R ″ CH 2 ) C = O → R ″ CH = C (NR 2 ) R ′ + H 2 O
Ikhtisar
| Nama reaksi | Produk reaksi | Komentar |
|---|---|---|
| Alkilasi amina | Amina | Tingkat substitusi meningkat |
| Reaksi Schotten – Baumann | Amide | Reagen: asil klorida , anhidrida asam |
| Reaksi Hinsberg | Sulfonamid | Reagen: sulfonil klorida |
| Amina-karbonil kondensasi | Imines | |
| Oksidasi organik | Senyawa nitroso | Reagen: asam peroxymonosulfuric |
| Oksidasi organik | Garam Diazonium | Reagen: asam nitrat |
| Reaksi Zincke | Zincke aldehyde | Reagen: garam piridinium , dengan amina primer dan sekunder |
| Emde degradasi | Amina tersier | Pengurangan kation amonium kuaterner |
| Penataan ulang Hofmann – Martius | Aryl-substituted anilines | |
| reaksi von Braun | Organocyanamide | Dengan pembelahan (amina tersier saja) dengan sianogen bromida |
| Penghapusan Hofmann | Alkene | Hasil oleh β-eliminasi karbon yang kurang terhalang |
| Hentikan reaksi | Alkene | Mirip dengan eliminasi Hofmann |
| reaksi carbylamine | Isonitril | Hanya amina primer |
| Tes minyak mustard Hoffmann | Isothiocyanate | CS 2 dan HgCl 2 digunakan. Bau tiosianat seperti mustar. |
3 ) adalah moieties bermuatan positif yang paling umum dalam protein , khususnya pada asam amino lisin . DNA polimer anionik biasanya terikat pada berbagai protein kaya amina. Selain itu, terminal bermuatan amonium primer pada lisin membentuk jembatan garam dengan gugus karboksilat dari asam amino lainnya dalam polipeptida , yang merupakan salah satu pengaruh utama pada struktur tiga dimensi protein.
Aplikasi amina
Pewarna
- Chlorpheniramine adalah antihistamin yang membantu meredakan gangguan alergi karena demam, demam dingin, kulit gatal, gigitan serangga dan sengatan.
- Chlorpromazine adalah obat penenang yang menenangkan tanpa menyebabkan tidur. Ini digunakan untuk meredakan kecemasan, kegembiraan, kegelisahan atau bahkan gangguan mental.
- Efedrin dan fenilefrin , seperti hidroklorida amina, digunakan sebagai dekongestan.
- Amphetamine , methamphetamine , dan methcathinone adalah amina psikostimulan yang terdaftar sebagai zat yang dikendalikan oleh DEA AS.
- Amitriptyline , imipramine , lofepramine dan clomipramine adalah antidepresan trisiklik dan amina tersier.
- Nortriptyline , desipramine , dan amoxapine adalah antidepresan trisiklik dan amina sekunder. (Tricyclics dikelompokkan berdasarkan sifat grup amina akhir pada rantai samping.)
- Tryptamines yang digantikan dan phenethylamines adalah struktur dasar utama untuk berbagai macam obat psychedelic .
Gugus Pelindung - Amina
Amina bereaksi dengan asam nitrat untuk memberikan garam diazonium. Garil diazonium tidak begitu penting karena terlalu labil. Anggota yang paling penting adalah turunan dari amina aromatik seperti anilin ("phenylamine") (A = aril atau naphthyl):
Anilin dan naftilamin membentuk garam diazonium yang lebih stabil, yang dapat diisolasi dalam bentuk kristal. Garam-garam diazonium mengalami berbagai transformasi berguna yang melibatkan penggantian gugus N2 dengan anion. Misalnya, sianida tembaga menghasilkan nitril yang sesuai:
Pasangan Aryldiazonium dengan senyawa aromatik yang kaya elektron seperti fenol untuk membentuk senyawa azo . Reaksi semacam itu secara luas diterapkan pada produksi pewarna.
Pembentukan imina adalah reaksi penting. Amina primer bereaksi dengan keton dan aldehida untuk membentuk imina . Dalam kasus formaldehyde (R ′ = H), produk-produk ini biasanya ada sebagai pemangkas siklus.
Pengurangan imina ini memberikan amina sekunder:
Demikian pula, amina sekunder bereaksi dengan keton dan aldehid untuk membentuk enamina :
Tinjauan tentang reaksi amina diberikan di bawah ini:
Amina ada di mana-mana dalam biologi. Kerusakan asam amino melepaskan amina, yang terkenal dalam kasus pembusukan ikan yang berbau trimetilamin . Banyak neurotransmiter adalah amina, termasuk epinefrin , norepinefrin , dopamin , serotonin , dan histamin . Kelompok amino terprotonasi ( –NH +
Amina aromatik primer digunakan sebagai bahan awal untuk pembuatan pewarna azo . Ini bereaksi dengan asam nitrat untuk membentuk garam diazonium, yang dapat mengalami reaksi kopling untuk membentuk senyawa azo. Karena senyawa azo sangat berwarna, mereka banyak digunakan dalam industri pencelupan, seperti:
Banyak obat dirancang untuk meniru atau mengganggu aksi neurotransmiter amina alami, yang dicontohkan oleh obat-obatan amina:
Aqueous monoethanolamine (MEA), diglycolamine (DGA), diethanolamine (DEA), diisopropanolamine (DIPA) dan methyldiethanolamine (MDEA) banyak digunakan secara industri untuk menghilangkan karbon dioksida (CO 2 ) dan hidrogen sulfida (H2S) dari gas alam dan kilang aliran proses. Mereka juga dapat digunakan untuk menghilangkan CO 2 dari gas pembakaran dan gas buang dan mungkin memiliki potensi pengurangan gas rumah kaca . Proses terkait dikenal sebagai pemanis .
Amina sederhana dengan berat molekul rendah, seperti etilamin , hanya memiliki toksisitas lemah dengan LD50 antara 100 dan 1000 mg / kg. Mereka adalah iritasi kulit, terutama karena beberapa mudah diserap melalui kulit. Amina adalah kelas senyawa yang luas, dan anggota kelas yang lebih kompleks bisa sangat bioaktif, misalnyastrychnine dan heroin .
Amina adalah senyawa organik dan gugus fungsi yang mengandung nitrogen basa dengan pasangan elektron bebas. Perlindungan nitrogen terus menarik banyak perhatian dalam bidang kimia, seperti peptida, nukleosida, polimer dan sintesis ligan. Tetapi, dalam beberapa tahun terakhir, sejumlah gugus pelindung nitrogen telah digunakan sebagai pembantu kiral. Dengan demikian, desain baru, lebih ringan dan metodenya lebih efektif untuk perlindungan nitrogen masih aktif dalam topik sintesis kimia.
Gugus Pelindung imida dan amida: Kelompok ftalimida telah berhasil digunakan untuk melindungi gugus amino. Pembelahan dari N-alkilftalimida (1,81) mudah dilakukan dengan hidrazin, dalam larutan panas atau dalam dingin untuk waktu yang lama untuk memberikan (1,82) dan amina. Basa katalis hidrolisis N-alkilftalimida (1.81) juga memberikan yang sesuai amina.
Modifikasi Kitosan
Adanya gugus amina (NH2) dan dan hidroksil (OH) dari kitosan menyebabkan kitosan mudah dimodifikasi secara kimia.
Gugus aktif pada kitosan
Gugus aktif pada kitosan
Bila dibutuhkan perubahan gugus fungsional untuk menghalangi gangguan dalam beberapa rangkaian reaksi sintesis, salah satu caranya adalah dengan menggunakan gugus pelindung. Gugus pelindung merupakan suatu turunan yang dapat dibuat dan kemudian dihilangkan. Tiga syarat-syarat yang perlu diperhatikan dalam memilih gugus pelindung adalah sebagai berikut :
1. Gugus pelindung yang digunakan harus lebih reaktif
2. Gugus pelindung yang dipakai harus dengan mudah bereaksi dengan molekul target.
3. Kondisi reaksi dalam memasukkan gugus pelindung harus stabil.
4. Dapat dimasukkan pada kondisi reaksi lunak
5. Gugus pelindung harus dapat dengan mudah dihilangkan tanpa menggangu reaksi akhir.
Reaksi penggunaan gugus pelindung pada kitosan dikarenakan kitosan memiliki 2 gugus fungsi yang kereaktifan berbeda. Gugus amino dari kitosan lebih reaktif dari pada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan, perlu dilakukan proteksi atau perlindungan terhadap gugus amino. Basa shiff dapat digunakan sebagai gugus pelindung pada reaksi O-asilasi.
Gugus amino kitosan lebih reaktif dari pada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan perlu dilakukan proteksi atau perlindungan terhadap gugus amin selama proses asilasi untuk menghasilkan O-Asil kitosan. Metode proteksi yang dilakukan antara lain melalui pembuatan basa Schiff disusul O-Asetilasi menggunakan larutan asetat anhidrin-piridin untuk mencegah hidrolisis asam dari basa Schiff. Reaksi antara kitosan dengan anhidrida asetat menghasilkan senyawa ester yang merupakan kitosan asetat. Dalam hal ini kitosan terlebih dahulu direaksikan dengan asetaldehida membentuk aldimin untuk melindungi gugus amina. Kitosan laurat diperoleh dari reaksi transesterifikasi antara metil laurat dengan kitosan asetat. Selanjutnya dilakukan deproteksi dengan menambahkan natrium bikarbonat untuk memperoleh kitosan laurat.
Basa Schiff dapat digunakan sebagai gugus pelindung pada gugus amin (NH2), dilakukan dengan melarutkan kitosan terasetilasi dalam asam formiat 90% yang mengandung asetat anhidrida dengan asumsi protonasi akan mencegah terjadinya N-asilasi. Selanjutnya direaksikan dengan asilklorida dalam karbon triklorida dan piridin kering.
Gugus amino, N dari kitosan lebih reaktif dari pada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan perlu dilakukan proteksi atau perlindungan terhadap gugus amino. Reaksi O-asilasi dapat dilakukan melalui reaksi esterifikasi menggunakan katalis asam sulfat (2 M) ditambahkan kepada suspensi campuran kitosan dan asam alkanoat pada suhu kamar. Campuran dipanaskan pada suhu 80oC selama 4 jam disertai pengadukan. Asam sulfat yang ditambahkan akan membentuk ion hidrogen sulfit sebagai konter ion dari NH3+, selanjutnya berfungsi untuk memproteksi (sebagai gugus pelindung) N-kitosan. Kemudian pada suhu kamar, tambahkan natrium hidrokarbonat sampai pH 7 (netral).
 Struktur umum imina
Struktur umum iminaNomenklatur dan klasifikasi
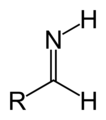



 Sintesis imina
Sintesis imina RNH 2 + R′C (O) R ′ ′ → RN = C (R ′) (R ′ ′) + H 2 O
Lebih banyak metode khusus
- Reaksi dari azida organik dengan logam carbenoid (diproduksi dari senyawa diazocarbonyl).
- Kondensasi asam karbon dengan senyawa nitroso .
- Penataan ulang trityl N-haloamines dalam penataan ulang Stieglitz .
- Dehidrasi hemiaminal .
- Dengan reaksi alkena dengan asam hidrazoat dalam reaksi Schmidt .
- Dengan reaksi asam nitril, asam klorida, dan aren dalam reaksi Hoesch .
- Sintesis multikomponen 3- tiazolina dalam reaksi Asinger .
- Ketimin primer dapat disintesis melalui reaksi Grignard dengan nitril .
Imina berkurang dalam aminasi reduktif .Reaksi yang paling penting dari imina adalah hidrolisis mereka ke senyawa amina dan karbonil yang sesuai. Jika tidak, gugus fungsi ini berpartisipasi dalam banyak reaksi lain, banyak yang analog dengan reaksi aldehida dan keton.
- Imina bereaksi dengan amina ke aminal , lihat misalnya sintesis cucurbituril .
- Sebuah imina bereaksi dengan diena dalam reaksi Aza Diels-Alder ke tetrahidropiridin.
- Imina dapat dioksidasi dengan asam meta-kloroperoksibenzoat (mCPBA) untuk memberikan oksaziridin
- Sebuah imina aromatik bereaksi dengan enol eter ke quinoline dalam reaksi Povarov .
- A tosylimine bereaksi dengan senyawa karbonil α, β-unsaturated ke amina alilik pada reaksi Aza-Baylis-Hillman .
- Imina adalah perantara dalam alkilasi amina dengan asam format dalam reaksi Eschweiler-Clarke .
- Penataan ulang dalam kimia karbohidrat yang melibatkan imina adalah penataan ulang Amadori .
- Reaksi transfer metilena dari imina oleh sulfonium ylide tidak stabil dapat memberikan sistem aziridine .
- Imina bereaksi, secara termal, dengan ketena dalam sikdisi siklik [2 + 2] untuk membentuk β-laktam dalam sintesis Staudinger .
- Sebuah imina dapat bereaksi dengan dialkilfosfit dalam reaksi Pudovik dan reaksi Kabachnik-Fields
Sebagai ligan
Pengurangan imina
Imine
Imina ( / ɪ ˈ m ː n / atau / ˈ ɪ m ɪ n / ) adalah gugus fungsi atau senyawa kimia yang mengandung ikatan rangkap karbon - nitrogen . Atom nitrogen dapat dilekatkan ke hidrogen (H) atau grup organik (R). Jika kelompok ini bukan atom hidrogen, maka senyawa tersebut kadang-kadang dapat disebut sebagai pangkalan Schiff . Atom karbon memiliki dua ikatan tunggal tambahan. Istilah "imine" diciptakan pada tahun 1883 oleh kimiawan Jerman Albert Ladenburg .
Biasanya imina mengacu pada senyawa dengan konektivitas R 2 C = NR, seperti yang dibahas di bawah ini. Dalam literatur yang lebih tua, imina mengacu pada analog aza dari epoksida. Dengan demikian, etilenimin adalah spesies cincin beranggota tiga C2H4 NH.
Imina terkait dengan keton dan aldehid dengan penggantian oksigen dengan kelompok NR. Ketika R = H, senyawa tersebut adalah imina primer, ketika R adalah hidrokarbil , senyawa tersebut adalah imina sekunder. Imina menunjukkan reaktivitas yang beragam dan biasanya ditemui di seluruh kimia. Ketika R 3 adalah OH, imine disebut oksime, dan ketika R 3 adalah NH 2 imina disebut hidrazon .
Imina primer di mana C melekat pada hidrokarbil dan H disebut aldimine primer ; imina sekunder dengan kelompok seperti ini disebut aldimine sekunder . Imina primer di mana C melekat pada dua hidrokarbil disebut ketimine primer ; imina sekunder dengan kelompok seperti ini disebut ketimin sekunder .
Salah satu cara menamai aldimines adalah dengan mengambil nama radikal, hapus "e" akhir, dan tambahkan "-imine", misalnya ethanimine . Lihat artikel aldimine untuk konvensi penamaan lainnya. Secara bergantian, sebuah imina dinamakan sebagai turunan dari karbonil, menambahkan kata "imina" ke nama senyawa karbonil yang gugus oksonya digantikan oleh kelompok imino , misalnya imon sydnone dan imina aseton (zat antara dalam sintesis). acetone azine ).
N-Sulfinyl imines adalah kelas khusus imina yang memiliki gugus sulfinil yang terikat pada atom nitrogen.
Imina biasanya disiapkan oleh kondensasi amina primer dan aldehida dan keton kurang umum:
Dalam hal mekanisme, reaksi tersebut dilanjutkan melalui penambahan nukleofilik memberikan hemiaminal -C (OH) (NHR) - menengah, diikuti dengan eliminasi air untuk menghasilkan imina. (lihat alkylimino-de-oxo-bisubstitution untuk mekanisme terperinci) Kesetimbangan dalam reaksi ini biasanya mendukung senyawa karbonil dan amina, sehingga distilasi azeotropik atau penggunaan agen dehidrasi, seperti saringan molekuler atau magnesium sulfat , diperlukan untuk mendorong reaksi yang mendukung pembentukan imina. Dalam beberapa tahun terakhir, beberapa reagen seperti Tris (2,2,2-trifluoroethyl) borat [B (OCH 2 CF 3 ) 3 ], pyrrolidine atau titanium ethoxide [Ti (OEt) 4 ] telah terbukti mengkatalisis pembentukan imina.
Beberapa metode lain ada untuk sintesis imina.
Agak seperti induk amina, imina sedikit bersifat basa dan dapat berefleksi secara reversibel untuk menghasilkan garam iminium. Turunan iminium sangat rentan terhadap reduksi ke amina menggunakan transfer hidrogenasi atau dengan aksi stoikiometrik natrium cyanoborohidrida . Karena imina yang berasal dari keton yang tidak simetris bersifat prokiral , reduksi mereka adalah metode yang berguna untuk sintesis amina kiral.
Imina adalah ligan umum dalam kimia koordinasi . Kondensasi salicylaldehyde dan ethylenediamine memberi keluarga agen chelating yang mengandung imine seperti salen .
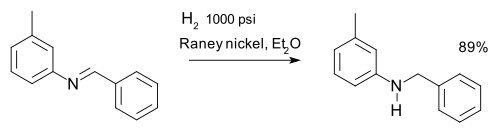
Imina dapat direduksi menjadi amina melalui hidrogenasi misalnya dalam sintesis m -tolylbenzylamine:
Zat pereduksi lain adalah lithium aluminium hidrida dan natrium borohidrida .
Asymmetric imine reduction pertama dilaporkan pada tahun 1973 oleh Kagan menggunakan Ph (Me) C = NBn dan PhSiH 2 dalam hidrosililasi dengan ligan kiral Katalis DIOPdan rhodium (RhCl (CH 2 CH 2 ) 2 ) 2 . Banyak sistem telah diselidiki.
Imina bersifat umum di alam. Vitamin B6 mempromosikan deaminasi asam amino melalui pembentukan imina, misalnya.








































Baiklah saya akan menjawab permasalahan nomor 2
BalasHapusGugus amino kitosan lebih reaktif daripada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan perlu dilakukan proteksi atau perlindungan terhadap gugus amin selama proses asilasi untuk menghasilkan O-Asil kitosan. Metode proteksi yang dilakukan antara lain melalui pembuatan basa Schiff disusul O-Asetilasi menggunakan larutan asetat anhidrin-piridin untuk mencegah hidrolisis asam dari basa Schiff. Reaksi antara kitosan dengan anhidrida asetat menghasilkan senyawa ester yang merupakan kitosan asetat. Dalam hal ini kitosan terlebih dahulu direaksikan dengan asetaldehida membentuk aldimin untuk melindungi gugus amina. Kitosan laurat diperoleh dari reaksi transesterifikasi antara metil laurat dengan kitosan asetat. Selanjutnya dilakukan deproteksi dengan menambahkan natrium bikarbonat untuk memperoleh kitosan laurat.
Saya akan mencoba menjawab permasalahan Anda yg pertama:
BalasHapusAmina adalah suatu senyawa yang mengandung gugusan amino. Gugusan amino mengandung nitrongen terikat kepada satu sampai tiga atom karbon (tetapi bukan gugusan karbonil) dan sejumlah atom hidrogen (tidak ada, satu atau dua). Apabila salah satu karbon yang terikat pada atom nitrogen adalah karbon karbonil, senyawanya adalah amida, bukan amina. Amina digolongkan menjadi amina primer (RNH2), sekunder (R2NH), atau tersier (R3N), tergantung kepada jumlah atom karbon yang terikat pada atom nitrogen (bukan pada atom karbon, seperti pada alkohol) (Achmadi, 2005).
halo dam!! saya akan menjawab pertanyaan nomor 2.
BalasHapusBila dibutuhkan perubahan gugus fungsional untuk menghalangi gangguan dalam beberapa rangkaian reaksi sintesis, salah satu caranya adalah dengan menggunakan gugus pelindung. Gugus pelindung merupakan suatu turunan yang dapat dibuat dan kemudian dihilangkan. Tiga syarat-syarat yang perlu diperhatikan dalam memilih gugus pelindung adalah sebagai berikut :
1. Gugus pelindung yang digunakan harus lebih reaktif
2. Gugus pelindung yang dipakai harus dengan mudah bereaksi dengan molekul target.
3. Kondisi reaksi dalam memasukkan gugus pelindung harus stabil.
4. Dapat dimasukkan pada kondisi reaksi lunak
5. Gugus pelindung harus dapat dengan mudah dihilangkan tanpa menggangu reaksi akhir.
Reaksi penggunaan gugus pelindung pada kitosan dikarenakan kitosan memiliki 2 gugus fungsi yang kereaktifan berbeda. Gugus amino dari kitosan lebih reaktif dari pada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan, perlu dilakukan proteksi atau perlindungan terhadap gugus amino. Basa shiff dapat digunakan sebagai gugus pelindung pada reaksi O-asilasi.
Gugus amino kitosan lebih reaktif daripada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan perlu dilakukan proteksi atau perlindungan terhadap gugus amin selama proses asilasi untuk menghasilkan O-Asil kitosan. Metode proteksi yang dilakukan antara lain melalui pembuatan basa Schiff disusul O-Asetilasi menggunakan larutan asetat anhidrin-piridin untuk mencegah hidrolisis asam dari basa Schiff. Reaksi antara kitosan dengan anhidrida asetat menghasilkan senyawa ester yang merupakan kitosan asetat. Dalam hal ini kitosan terlebih dahulu direaksikan dengan asetaldehida membentuk aldimin untuk melindungi gugus amina. Kitosan laurat diperoleh dari reaksi transesterifikasi antara metil laurat dengan kitosan asetat. Selanjutnya dilakukan deproteksi dengan menambahkan natrium bikarbonat untuk memperoleh kitosan laurat.
Malam saudari dame
BalasHapusSaya akan menjawab permaslahan kedua
Amina adalah senyawa organik dan gugus fungsi yang mengandung nitrogen basa dengan pasangan elektron bebas. Perlindungan nitrogen terus menarik banyak perhatian dalam bidang kimia, seperti peptida, nukleosida, polimer dan sintesis ligan. Tetapi, dalam beberapa tahun terakhir, sejumlah gugus pelindung nitrogen telah digunakan sebagai pembantu kiral. Dengan demikian, desain baru, lebih ringan dan metodenya lebih efektif untuk perlindungan nitrogen masih aktif dalama topik sintesis kimia.
Saya akan menjawab permasalahan yg ke tiga, yg mana Imina disebut sebagai pangkalan schift adalah gugus fungsi turunan amina. Sebuah kelas senyawa yang merupakan produk dari reaksi kondensasi aldehida atau keton dengan amonia atau amina, mereka memiliki radikal NH terikat pada atom karbon dengan ikatan ganda, R_HC_NH, contoh adalah benzaldimine. Pada reaksi Mannich, amonia atau amina primer atau sekunder digunakan untuk aktivasi formaldehida.
BalasHapusImina disebut juga Schiff-bases, merupakan molekul yang berguna baik secara biologi dan sintesis. Secara fisiologi, imina merupakan senyawa esensial dari berbagai system, seperti penglihatan dan beberapa reaksi enzimatis. Sintesis imina merupakan reaksi penting antara atom nitrogen nukleofilik dari amina primer dan karbonil elektrofilik dari aldehid atau keton. Melalui serangan kondensasi menghasilkan elektrofilik imina pada reaksi tersebut, kelompok ester meningkatkan sifat elektrofilik pada imina (Bennett, 2006). Amina primer bereaksi dengan aldehid atau keton untuk menghasilkan imina disebut juga reaksi Schiff-base. Atom nitrogen nukleofilik dari amina primer bereaksi dengan atom karbon elektrofilik dari golongan karbonil dengan seiring pergerakan electron π ke atom.
Saya akan menjawab pertanyaan no 2 Metode proteksi yang dilakukan antara lain melalui pembuatan basa Schiff disusul O-Asetilasi menggunakan larutan asetat anhidrin-piridin untuk mencegah hidrolisis asam dari basa Schiff. Reaksi antara kitosan dengan anhidrida asetat menghasilkan senyawa ester yang merupakan kitosan asetat. Dalam hal ini kitosan terlebih dahulu direaksikan dengan asetaldehida membentuk aldimin untuk melindungi gugus amina. Kitosan laurat diperoleh dari reaksi transesterifikasi antara metil laurat dengan kitosan asetat. Selanjutnya dilakukan deproteksi dengan menambahkan natrium bikarbonat untuk memperoleh kitosan laurat.
BalasHapusSaya akan mencoba menjawab permasalahan Anda yg pertama:
BalasHapusAmina adalah suatu senyawa yang mengandung gugusan amino. Gugusan amino mengandung nitrongen terikat kepada satu sampai tiga atom karbon (tetapi bukan gugusan karbonil) dan sejumlah atom hidrogen (tidak ada, satu atau dua). Apabila salah satu karbon yang terikat pada atom nitrogen adalah karbon karbonil, senyawanya adalah amida, bukan amina. Amina digolongkan menjadi amina primer (RNH2), sekunder (R2NH), atau tersier (R3N), tergantung kepada jumlah atom karbon yang terikat pada atom nitrogen (bukan pada atom karbon, seperti pada alkohol) (Achmadi, 2005).
Saya akan menjawab pertanyaan no 2 Metode proteksi yang dilakukan antara lain melalui pembuatan basa Schiff disusul O-Asetilasi menggunakan larutan asetat anhidrin-piridin untuk mencegah hidrolisis asam dari basa Schiff.
BalasHapusTiga syarat-syarat yang perlu diperhatikan dalam memilih gugus pelindung adalah sebagai berikut :
BalasHapus1. Gugus pelindung yang digunakan harus lebih reaktif
2. Gugus pelindung yang dipakai harus dengan mudah bereaksi dengan molekul target.
3. Kondisi reaksi dalam memasukkan gugus pelindung harus stabil.
4. Dapat dimasukkan pada kondisi reaksi lunak
5. Gugus pelindung harus dapat dengan mudah dihilangkan tanpa menggangu reaksi akhir.
Reaksi penggunaan gugus pelindung pada kitosan dikarenakan kitosan memiliki 2 gugus fungsi yang kereaktifan berbeda.
Saya akan menjawab pertanyaan no 2 Metode proteksi yang dilakukan antara lain melalui pembuatan basa Schiff disusul O-Asetilasi menggunakan larutan asetat anhidrin-piridin untuk mencegah hidrolisis asam dari basa Schiff.
BalasHapusSaya akan menjawab pertanyaan no 2 Metode proteksi yang dilakukan antara lain melalui pembuatan basa Schiff disusul O-Asetilasi menggunakan larutan asetat anhidrin-piridin untuk mencegah hidrolisis asam dari basa Schiff.
BalasHapusSaya akan menjawab permaslahan kedua
BalasHapusAmina adalah senyawa organik dan gugus fungsi yang mengandung nitrogen basa dengan pasangan elektron bebas. Perlindungan nitrogen terus menarik banyak perhatian dalam bidang kimia, seperti peptida, nukleosida, polimer dan sintesis ligan. Tetapi, dalam beberapa tahun terakhir, sejumlah gugus pelindung nitrogen telah digunakan sebagai pembantu kiral. Dengan demikian, desain baru, lebih ringan dan metodenya lebih efektif untuk perlindungan nitrogen masih aktif dalama topik sintesis kimia.
Nomor 2
BalasHapusGugus amino kitosan lebih reaktif daripada gugus hidroksilnya, sehingga untuk menghasilkan O-asilasi kitosan perlu dilakukan proteksi atau perlindungan terhadap gugus amin selama proses asilasi untuk menghasilkan O-Asil kitosan. Metode proteksi yang dilakukan antara lain melalui pembuatan basa Schiff disusul O-Asetilasi menggunakan larutan asetat anhidrin-piridin untuk mencegah hidrolisis asam dari basa Schiff.